Projekte unter der Leitung von Dr. Alexandra Koch
Unsere Arbeitsgruppe untersucht die zelluläre Kommunikation im Zusammenhang mit Krebserkrankungen. Zum einen interessieren uns direkte Zell-Zell-Kontakte zwischen Krebszellen und dem umliegenden Gewebe, die wir mit Hilfe von dreidimensionalen Kultursystemen darzustellen versuchen. Zum anderen arbeiten wir an Signalen von Rezeptortyrosinkinasen und ihrer Funktion in gesundem Gewebe und in Krebs.
Bachelor- und Masterarbeiten: Sprechen Sie uns gern an!
1) Zell-Zell-Kontakte in Organoiden
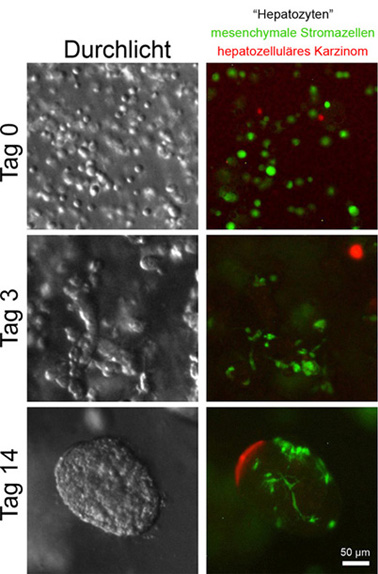
Bei der Krebsentwicklung versucht das umgebende Gewebe (tumor microenvironment) zuerst, das Tumorwachstum zu unterdrücken. Überwindet der Tumor diese Mechanismen, verändert er die Gewebeumgebung so, dass sie sein Wachstum unterstützt. Unsere Arbeitsgruppe untersucht die Kommunikation zwischen Krebszellen und dem umliegenden Gewebe mit Hilfe von dreidimensionalen (3D) Kultursystemen, die sich aus verschiedenen Zelltypen zusammensetzen (heterotypische 3D-Kultur, Organoid). Gießt man die Zellen in Extrazellulärmatrix ein, finden sie sich zusammen und organisieren sich selbstständig zu multizellulären Strukturen, wie auf der Abbildung gezeigt. Die Morphologie dieser multizellulären Strukturen verändert sich drastisch abhängig von der Kombination an Zelltypen, aber auch durch lösliche Signalmoleküle wie Wachstumsfaktoren oder Cortisol in verschiedenen Zellkulturmedien. Kombinationen von direktem Kontakt und löslichen Signalen haben zudem entscheidenden Einfluss auf das Überleben der mesenchymalen Stromazellen in der heterotypischen 3D-Kultur, nicht jedoch in der herkömmlichen Kultur in der Petri-Schale.
Zurzeit charakterisieren wir auf molekularer Ebenen mit Hilfe von zellbiologischen Methoden und Transkriptom-Analysen, wie sich die verschiedenen Zellen gegenseitig beeinflussen und welche dieser molekularen Veränderungen wiederum durch Cortisol moduliert werden.
2) Signale der intrazellulären Domäne von CSF-1R
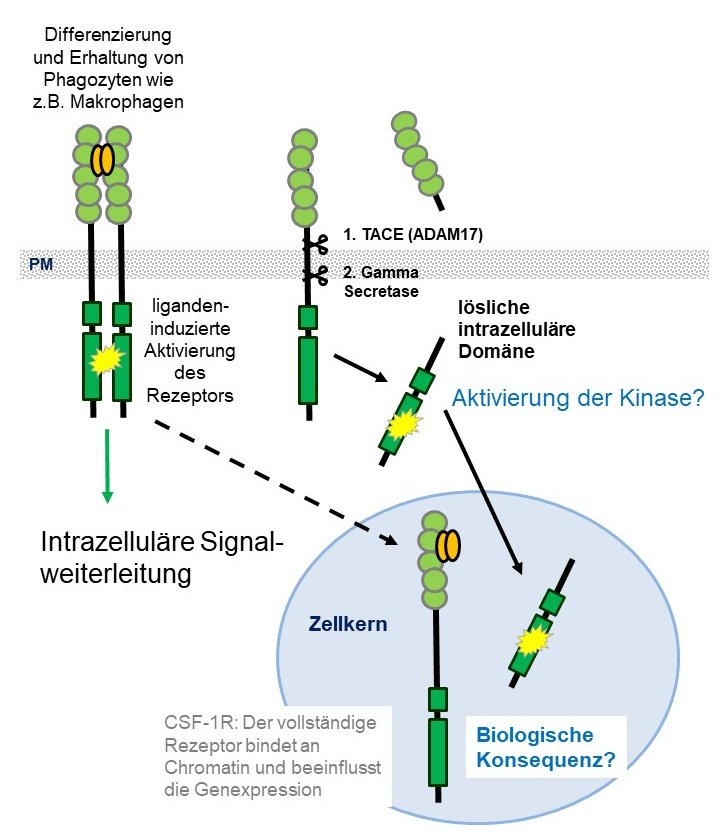
Rezeptortyrosinkinasen finden sich oft als „oncogenic driver“ in mutierter Form oder aberrant exprimiert in vielen Arten von Krebs. Ihr Signal, ausgelöst vom passenden Liganden von der Plasmamembran aus, ist bereits gut charakterisiert. Bei einigen Rezeptoren wird jedoch durch proteolytische Spaltung die intrazelluläre Kinasedomäne in der Zelle freigesetzt. Zudem findet man sowohl vollständige Rezeptoren als auch die intrazellulären Domänen im Zellkern. Ob und wie sich Signale über diese Wege vom klassischen liganden-induzierten Signal unterscheiden, ist wenig bekannt, ebenso wie ihre Rolle Krebszellen. Ein Beispiel für derartige Signale ist der Makrophagen-Kolonie-stimulierende Faktor-Rezeptor CSF-1R, der normalerweise nur in Phagozyten exprimiert wird, aber aberrant auch in epithelialen Krebszellen gefunden wird. Wir konnten zeigen, dass der Rezeptor in epithelialen Krebszellen zu deren Überleben unter bestimmten Krebsmedikamenten beitragen könnte. Im Moment untersuchen wir den Mechanismus, wie die intrazelluläre Domäne in den Zellkern gelangt und welche Rolle ihre Kinasefunktion dort spielt.