Projektvorstellung 2020
cAMP-dependent regulation of HCN4 controls the tonic entrainment process in sinoatrial node pacemaker cells
Fenske S, Hennis K, Roetzer R, Brox V, Becirovic E, Scharr A, Gruner C, Ziegler T, Mehlfeld V, Brennan J, Efimov I, Pauza A, Moser M, Wotjak C, Kupatt C, Goenner R, Zhang R, Zhang H, Zong X, Biel M*, Wahl- Schott* C.
Schrittmacherkanäle sind Vertreter der Hyperpolarisations-aktivierten und Zyklonukeotid-gesteuerten (hyperpolarization-activated cyclic nucleotide-gated, HCN) Kationenkanäle und gelten als wesentliche Motoren für die Entstehung des Herzschlags im Sinusknoten (SAN) des Herzens. Vier Vertreter, HCN1-HCN4 kommen beim Menschen und der Maus vor. HCN4 stellt die Haupt-Isoform dar und wird im gesamten SAN exprimiert. HCN Kanäle werden durch Hyperpolarisation geöffnet. Zusätzlich wird die Aktivierung der Kanäle durch zyklisches Adenosinmonophosphat (cAMP) reguliert. Dabei führt eine Erhöhung der intrazellulären cAMP-Konzentration, wie sie bei einer Aktivierung des Sympathikus auftritt, zu einem Anstieg der HCN Kanal-Aktivität. Im Forschungsbericht 2021 stellen wir ein Projekt vor, das in der Gruppe des Physiologen und Pharmakologen Christian Wahl-Schott vom Institut für Neurophysiologie der MHH in Zusammenarbeit mit den Pharmakologen Stefanie Fenske und Martin Biel des Lehrstuhls Pharmakologie für Naturwissenschaften am Department Pharmazie der LMU München durchgeführt und im Journal Nature Communications publiziert wurde. In der Arbeit haben die Autoren herausgefunden, wie der sekundäre Botenstoff cAMP über eine Wirkung an HCN4 Kanälen den Herzschlag reguliert.
Um die Rolle der cAMP-abhängigen Regulation (cAMP-dependent regulation, CDR) von HCN4 zu untersuchen, hat das Forschungsteam Knock-in Mäuse hergestellt, bei denen cAMP nicht mehr an HCN4 binden kann (HCN4FEA Mauslinie). Bei der Untersuchung einzelner Schrittmacherzellen aus dem SAN haben die Wissenschaftler entdeckt, dass SAN Zellen nicht nur einen schon lange bekannten Aktivitätsmodus einnehmen können, in dem die Zellen Aktionspotentiale feuern und den Herzschlag antreiben (firing mode), sondern auch einen non-firing mode einnehmen können, in dem die Zellen einen Zeitraum von bis zu einer Minute stillstehen. Im Netzwerk des Sinusknotens wird die Anzahl der Zellen im non-firing mode durch die CDR eingestellt. Schrittmacherzellen im non-firing mode fungieren im Netzwerk des SAN als „Bremsen“, die die Aktivität benachbarter Schrittmacherzellen im firing mode inhibieren. Es ist bekannt, dass inhibitorische Elemente generell die Stabilität von elektrisch aktiven Netzwerken erhöhen. Im Gehirn stabilisieren beispielsweise inhibitorische Neurone die Aktivität neuronaler Netzwerkverbindungen.
Video: Schlagender Vorhof mit Sinusknotenregion in einer Präparation aus der Maus.
Die aktuelle Arbeit zeigt, dass eine inhibitorische Kontrolle der Erregbarkeit auch im Sinusknoten für eine stabile Herzschrittmacherfunktion erforderlich ist. Sowohl die Überaktivität als auch der Mangel an hemmender Kontrolle führt zu einer massiven Störung der Schrittmacherfunktion des Herzens, die sich als „Kranker Sinusknoten“ Syndrom (Sick-Sinus-Syndrom) manifestiert (siehe Abbildung). Über die CDR von HCN4 kann die genaue Dosis für eine Hemmung innerhalb des Sinusknotens situationsgerecht eingestellt werden. Dadurch kann die Herzfrequenz effektiv stabilisiert werden und sowohl einer Bradykardie als auch einer Tachyarrhythmie entgegengewirkt werden.
Zusammengefasst zeigt diese Studie, dass die CDR von HCN4 für die Steuerung des SAN durch das autonome Nervensystem wichtig ist und zwar insbesondere für einen sicheren Übergang von einer stabilen Ausgangsherzfrequenz zu einer neuen Zielfrequenz bei sympathischer und/oder parasympathischer Aktivität. Besonders wichtig scheint die CDR von HCN4 bei der Feinjustierung des Herzfrequenz-senkenden Effekts des parasympathischen Nervensystems zu sein. Die CDR wirkt dabei einer parasympathischen Übersteuerung, unangemessenem Herzfrequenz-Abfall und dem Auftreten einer Bradykardie entgegen.
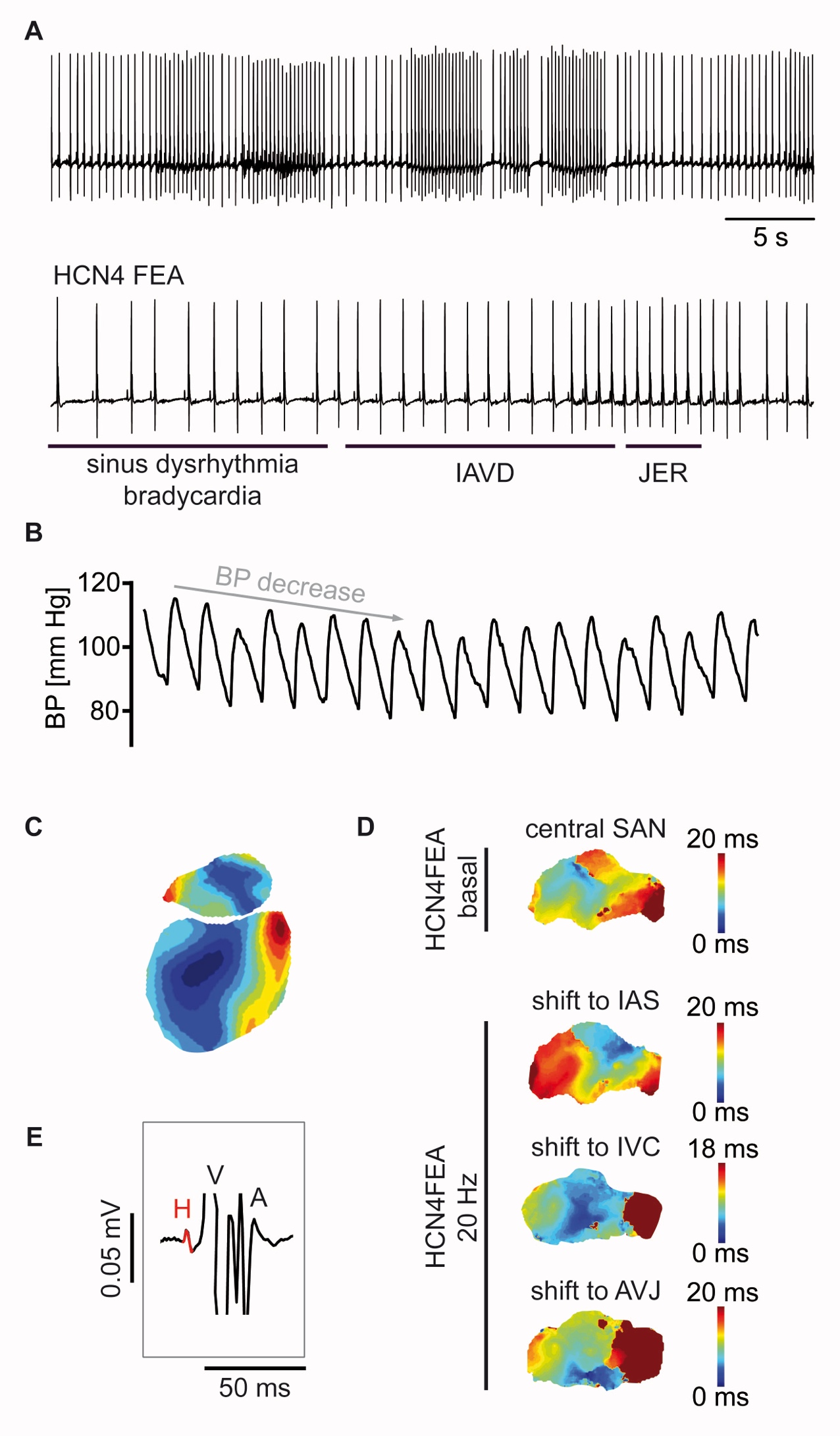
Abbildung: cAMP stabilisiert den Herzschlag über eine direkte Wirkung auf HCN Kanäle und erhöht die Präzision der dynamischen Herzfrequenzregulation durch das autonome Nervensystem. A, Das Fehlen der cAMP-abhängigen Regulation (CDR) von HCN4 Schrittmacherkanälen in HCN4FEA Knock-in Mäusen führt zu einer Bradykardie, Sinusdysrhythmie, und zu sekundären Rhythmusstörungen wie der isorhythmischen AV Dissoziation (IAVD) und junktionalen Ersatzrhythmen (JER) sowie zu junktionalen Tachykardien. Diese Rhythmusstörungen führen zu einer hämodynamisch relevanten Verminderung des Herzzeitvolumens, sowie zu drastischen Fluktuationen des arteriellen Blutdrucks (B). C, Optische Kartierung der Erregungsausbreitung im ganzen Herzen einer Wildtyp (WT) Maus. D, Optische Kartierung der Erregungsausbreitung im Sinusknoten. Oben: reguläre Ausbreitung der elektrischen Erregung in einem Sinusknotenpräparat einer HCN4FEA Maus. Die blaue Region stellt den Ort der frühesten Erregung im Sinusknoten dar (leading pacemaker region, LPR). In WT Mäusen ist die Lokalisation der LPR stabil (nicht gezeigt). Unten: Bei Sinusknotenpräparaten von HCN4FEA Mäusen kommt es zu dynamischen Verlagerungen der LPR, in Richtung des intraatrialen Septums (IAS), der Vena cava inferior (IVC) und/oder der AV junction (AVJ). Dies zeigt eine instabile Erregungsbildung im Sinusknoten von HCN4FEA Mäusen an. E, intrakardiales in vitro EKG mit His-Bündel-Elekrogramm zur Differenzierung und Quantifizierung von Phasen mit anterograder und retrograder AV-Überleitung. Darüber hinaus wurden in der Studie Echokardiographie, Rechtsherzkatheteruntersuchung zur Ableitung intrakardialer EKGs und zur Kartierung des Erregungsleitungssystems sowie zur programmierten Vorhof- und Ventrikelstimulation, Linksherzkatheteruntersuchung zur Quantifizierung hämodynamischer Parameter, konfokales Calcium- und Spannungs-Imaging, EKG- und Blutdrucktelemetrie, Spektralanalysen der Herzfrequenzvariabilität sowie die Charakterisierung der Baroreflex-Sensitivität eingesetzt und mit zellulären Techniken wie Patch-Clamp kombiniert.
Link zum Artikel
Nature Communications 2020 11:5555. doi: 10.1038/s41467-020-19304-9.
Herausgeber:
Präsident der MHH
Herr Prof. Dr. med. Michael P. Manns
Forschungsdekan der MHH
Herr Prof. Dr. med. Frank M. Bengel
Bearbeitung und Ansprechpartner:
Forschungsdekanat der Medizinischen Hochschule Hannover
Petra Linke
Telefon: 0511/ 532– 6023
Fax: 0511/ 532– 6024
E-Mail: linke.petra@mh-hannover.de
Gestaltung:
Digitale Medien, Medizinischen Hochschule Hannover
Telefon: 05 11/ 532– 2963
Online Umsetzung:
Forschungsdekanat, Medizinische Hochschule Hannover
Jan Tauwaldt
und
Petra Linke
Telefon: 0511/ 532- 6023
Forschungsbericht
Hier finden Sie den mit Hilfe des Forschungsinformationssystems (FIS) erstellten Forschungsbericht. Wie in den vergangenen Jahren möchten wir hier die Gelegenheit nutzen, explizit ein Projekt stellvertretend vorzustellen.
Forschungsinformationssystem (FIS)Hier finden Sie weitere Informationen zum Forschungsinformationssystem (FIS).
Hochschulbibliographie