Weitere Nachrichten auf der Startseite
Additiver Therapeutischer Plasmaaustausch beim septischen Schock
Sepsis ist die schwerste Verlaufsform einer jeden Infektion. Hierbei ist der septische Schock (Sepsis mit schwerem Kreislaufversagen) die Hauptursache für das Versterben von Patienten auf (nicht-kardiologischen) Intensivstationen. Der septische Schock sowie das hiermit verbundene Multiorganversagen werden durch eine überschiessende Reaktion des menschlichen Organismus auf die initiale Infektion ausgelöst. Eine Reinigung des Blutes zur direkten Behandlung dieser pathologischen Reaktion stellt deshalb ein verlockendes therapeutisches Konzept dar.
Letztes Jahr berichtete die Arbeitsgruppe «Translationale Intensivmedizin» über die Ergebnisse einer randomisierten, kontrollierten Pilotstudie, in welcher ein additiver Therapeutischer Plasmaaustausch (Therapeutic Plasma Exchange (TPE)) bei Patienten mit schwerem refraktärem septischem Schock untersucht wurde. In dieser Studie wurden 40 Patienten mit frühem (< 24 Stunden) und schwerem (Noradrenalindosis > 0.4 μg/kg/min) septischem Schock zu einer Standardtherapie bzw. einem einmaligem TPE mit Plasma als Substitutionslösung randomisiert. Es wurde eine rasche hämodynamische Verbesserung in der TPE im Vergleich zur Vergleichsgruppe festgestellt. Diese Ergebnisse wurden in der renommierten Fachzeitschrift Intensive Care Medicine veröffentlicht.
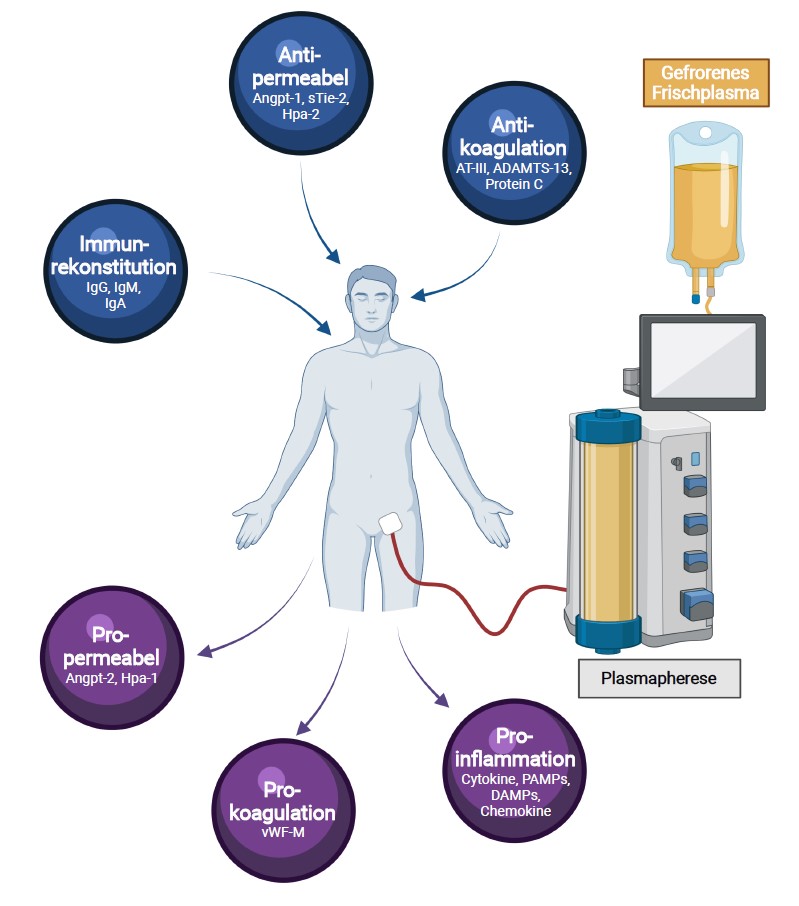
Potentielle molekulare Erklärungen, warum TPE im frühen und schweren septischen Schock zu einer raschen Kreislaufstabilisierung führt, und Hinweise darauf, bei welchen Patienten genau dies vor allem zu erwarten ist, zeigt nun eine weitere Studie des gleichen Forscherteams auf, welche kürzlich in der Fachzeitschrift Critical Care veröffentlicht wurde. Bei dem TPE gelingt nämlich die Kombination von zwei therapeutischen Maßnahmen in einem einzigen Eingriff: Zum einen werden vermehrt vorliegende schädliche Mediatoren, wie pro-inflammatorische Zytokine, Endothel-destabilisierende Faktoren (z. B. Angiopoietin-2, sTie2, Heparanase-1) und Moleküle, die an der intravasalen Gerinnung beteiligt sind (z. B. von-Willebrand-Faktor) effektiv entfernt. Gleichzeitig führt der Austausch des septischen Plasmas mit dem Plasma gesunder Spender zu einer Auffüllung von schützenden, aber bereits in der Frühphase der Sepsis verbrauchten, Faktoren, die an entzündungshemmenden Prozessen (z.B. Immunglobuline), an der Stabilisierung des Endothels (z.B. Angiopoietin-1, Heparanase-2) und an der endogenen Gerinnungshemmung (z.B. Antithrombin-III, Protein C, ADAMTS-13) beteiligt sind. Es ist somit möglich, dass TPE auf vielfältige Weise zu einer Verbesserung der Durchblutung in den kleinen Gefäßen (sogenannte Mikrozirkulation) führt. Interessanterweise profitierten vor allem Patienten mit den höchsten Lactat-Blutkonzentrationen (Zeichen der schwersten Mikrozirkulationsstörung) von der Einleitung einer additiven Behandlung mit TPE.
Bisher ist der Nutzen eines additiven TPE beim septischen Schock im Hinblick auf das Überleben der Patienten allerdings weiter ungeklärt. Eine größere randomisierte Studie, die den additiven Einsatz von TPE bei septischem Schock untersuchen wird, ist bereits von einem Team der Medizinischen Hochschule (MHH, PD Dr. K. Stahl), der Uniklinik Bonn (UKB, PD Dr. C. Bode) sowie dem Universitätsspital Zürich (USZ, Prof. Dr. S. David) gemeinsam geplant (EXCHANGE Studie mit Beteiligung von 22 Zentren in Deutschland und der Schweiz).
Weitere Informationen erhalten Sie bei PD Dr. Klaus Stahl, stahl.klaus@mh-hannover.de, Telefon 0511-532-3305
Zum Originalartikel:
1. Clinical and biochemical endpoints and predictors of response to plasma exchange in septic shock: results from a randomized controlled trial. Stahl K, Wand P, Seeliger B, Wendel-Garcia PD, Schmidt JJ, Schmidt BMW, Sauer A, Lehmann F, Budde U, Busch M, Wiesner O, Welte T, Haller H, Wedemeyer H, Putensen C, Hoeper MM, Bode C, David S. Crit Care. 2022 May 12;26(1):134. doi: 10.1186/s13054-022-04003-2. PMID: 35551628 Free PMC article. Clinical Trial.
2. Adjuvant therapeutic plasma exchange in septic shock. David S, Bode C, Putensen C, Welte T, Stahl K; EXCHANGE study group. Intensive Care Med. 2021 Mar;47(3):352-354. doi: 10.1007/s00134-020-06339-1. Epub 2021 Jan 20. PMID: 33471132 Free PMC article. No abstract available.
