Neuronale Plastizität bei Neuroinflammation – Unser Forschungsschwerpunkt
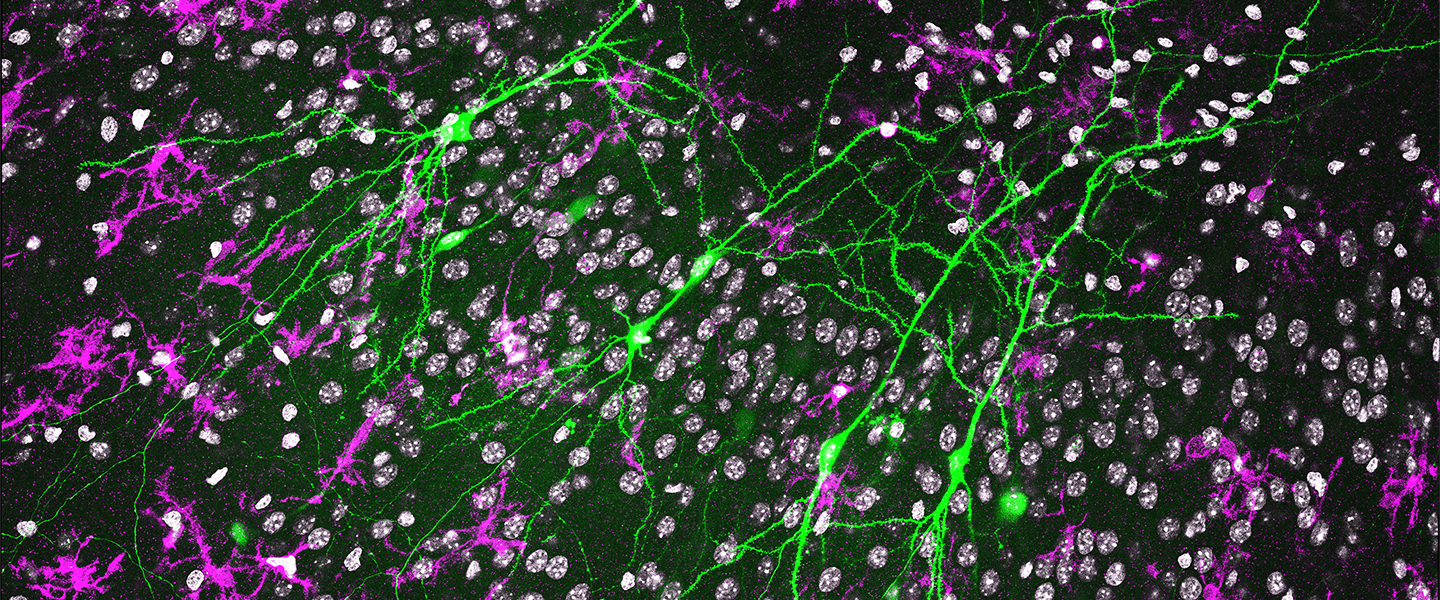
Das zentrale Nervensystem besteht aus verschiedenen Zelltypen, darunter Neurone, Mikroglia, Astrozyten und Oligodendrozyten, die ständig miteinander in Austausch stehen. Dieses Zusammenspiel ist Voraussetzung für eine normale Gehirnfunktion, und der Funktionszustand der Zellen wird sehr genau reguliert. Werden diese Interaktionen durch körpereigene Faktoren (z. B. metabolischer Stress, Degeneration) oder äußere Einflüsse (z. B. Infektionen, Verletzungen, Störungen der Sinneswahrnehmung) gestört, entsteht eine Neuroinflammation. Die Entzündung von Nervengewebe kann krankhafte Netzwerkzustände auslösen, etwa synaptische Fehlfunktionen und Veränderungen der Membranerregbarkeit, und so zur Entstehung neurologischer oder psychiatrischer Symptome beitragen. Unsere Forschungsfragen folgen daher der Hypothese, dass Neuroinflammation ein zentraler krankheitsauslösender Faktor bei vielen Erkrankungen ist.
Unsere Mission ist die Identifikation neuer therapeutischer Ansätze, die auf entzündungsbedingte Störungen der synaptischen Transmission, Plastizität und Membranerregbarkeit abzielen.
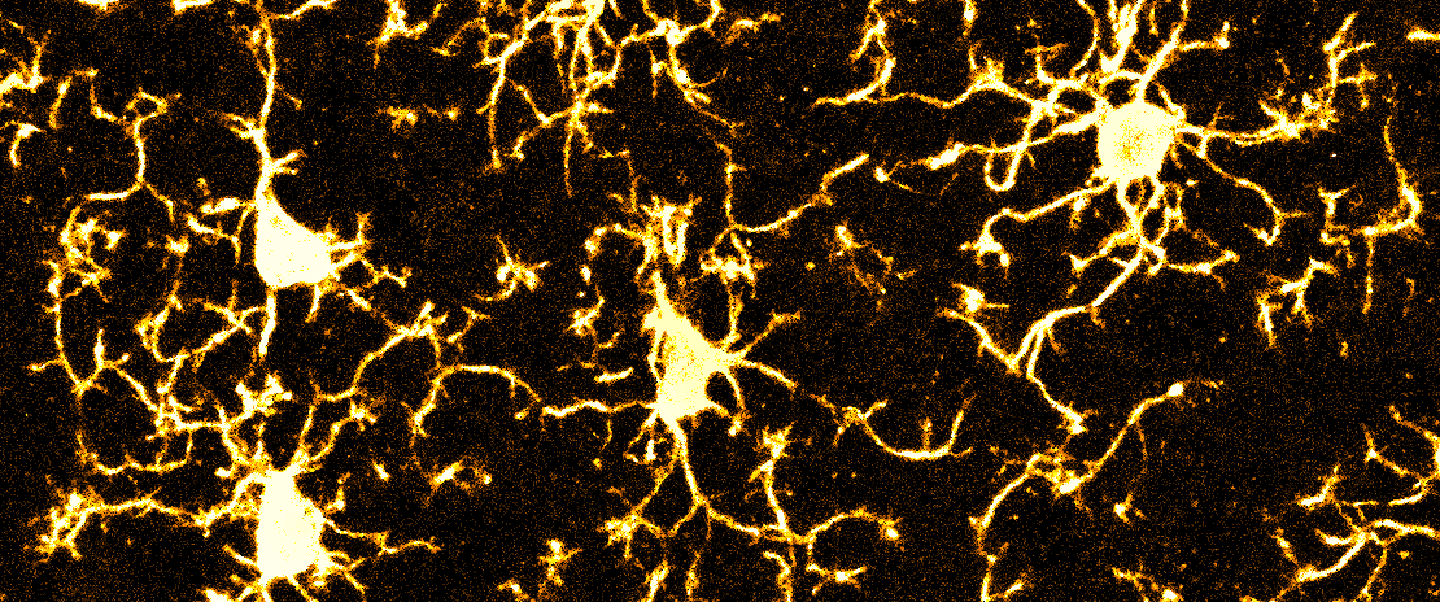
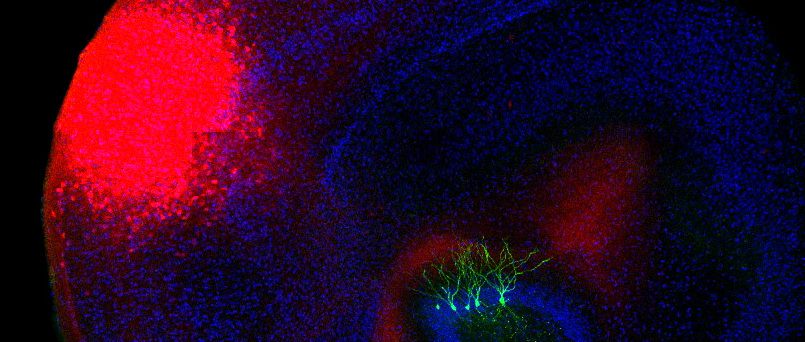
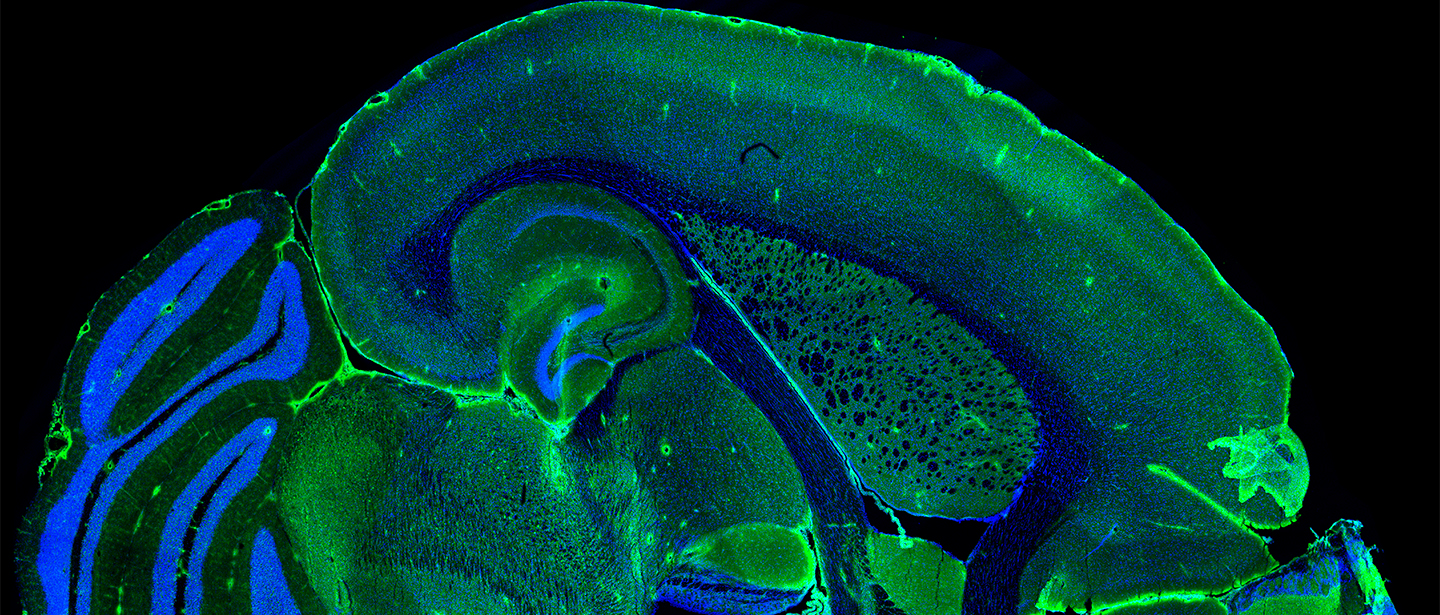
Wir untersuchen die Rolle von Neuro-Immun-Interaktionen über kurze und lange Distanzen – von lokalen Veränderungen im zentralen Nervensystem bis hin zu Gehirn-Körper-Interaktionen. Ein besonderer Fokus liegt auf Gliazellen – insbesondere Mikroglia als den residenten Immunzellen des Gehirns – und ihrer Rolle bei der Gestaltung struktureller und funktioneller Eigenschaften anderer Zellen im Gehirn. Gliazellen sind hochdynamische Zellen, die sowohl im Ruhezustand als auch unter entzündlichen Bedingungen über lösliche Faktoren und/oder direkte Kontaktstellen mit Neuronen interagieren. Darüber hinaus interessieren uns zelluläre Signalwege in Neuronen, die deren Empfindlichkeit gegenüber Entzündungsreizen bestimmen. Zentrale Themen unserer Forschung sind:
- Glia-Neuron-Interaktionen und ihre Rolle bei der Aufrechterhaltung synaptischer Gesundheit sowie bei der Vermittlung synaptischer Fehlfunktionen während Neuroinflammation unterschiedlicher Ursache.
- Synaptische Ressourcen – entscheidend für die Anpassungsfähigkeit von Synapsen in größerer Entfernung vom Soma – als Zielstrukturen von Neuroinflammation.
- Das Zusammenspiel von Zytokinen, Glia und Neuronen bei der Weitergabe peripherer Veränderungen an Synapsen.
- Der Teufelskreis aus Entzündung und Degeneration.
In all unseren Forschungsprojekten entwickeln wir In-vitro-Modelle („Advanced Tissue Culture Models“), die explorative Experimente an lebenden Tieren möglichst vermeiden und damit dem 3R-Prinzip entsprechen.
Forschungsschwerpunkte / Teams:
- Neuroinfektion und Immunität: Dr. med. Amelie Eichler (Eichler.Amelie@mh-hannover.de)
- Neurodegeneration: Dr. med. Pia Kruse (Kruse.Pia@mh-hannover.de)
- Neuronaler Stress: Dr. rer. nat. Fabian Gather (Gather.Fabian@mh-hannover.de)
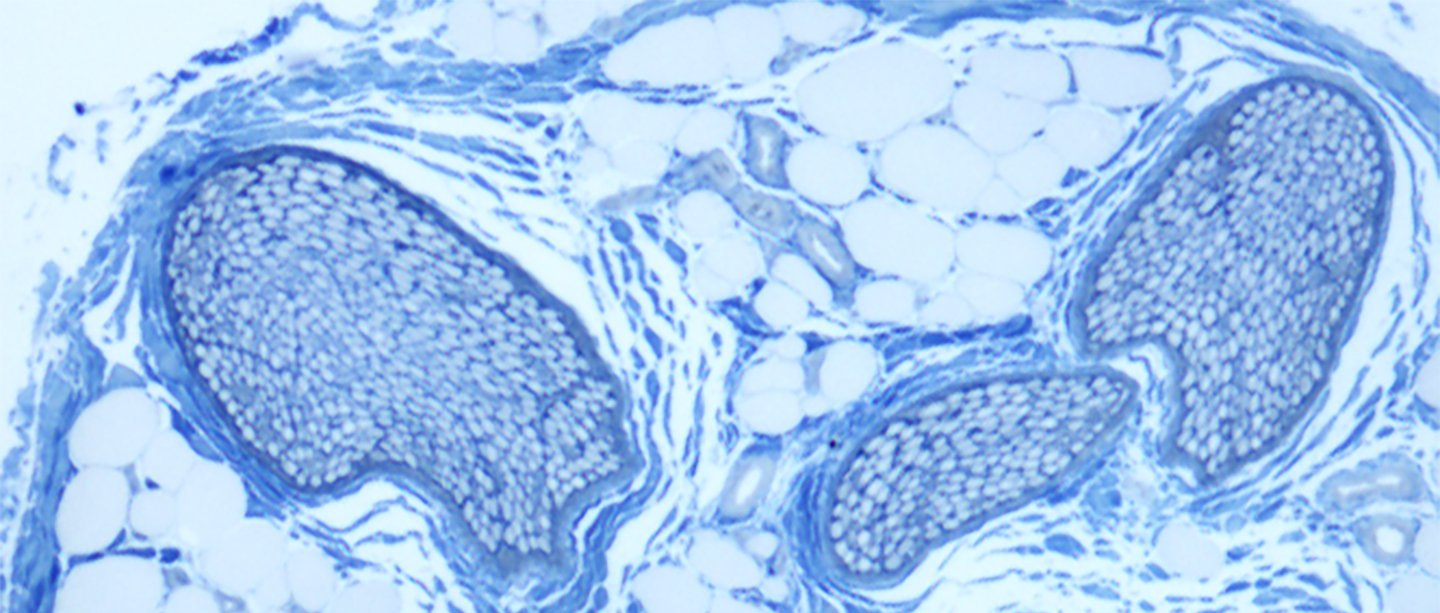
- Periphere Nerven: Prof. Dr. Kirsten Haastert-Talini (Haastert-Talini.Kirsten@mh-hannover.de)
Kooperationspartner*innen (alphabetisch):
- Dr. Marijana Basic (Gnotobiology Facility, Institute for Laboratory Animal Science, MHH)
- Prof. Dr. Nataliya Di Donato (Department of Human Genetics, MHH)
- Prof. Dr. Lars Dölken (Institute of Virology, MHH)
- Prof. Dr. Gisa Gerold (Institute of Virology, Innsbruck)
- Prof. Dr. Ulrich Kalinke (Twincore)
- Prof. Dr. Joachim Krauss (Department of Neurosurgery, MHH)
- Prof. Dr. Aiden Haghikia (Department of Neurology with Clinical Neurophysiology, MHH)
- Prof. Dr. Florian Heidel (Department of Hematology, Hemostasis, Oncology and Stem Cell Transplantation, MHH)
- Prof. Dr. Evgeni Ponimaskin (Institute of Neurophysiology, MHH)
- Prof. Dr. Franziska Richter Assencio (Department of Pharmacology, Toxicology, and Pharmacy, University of Veterinary Medicine Hannover)
- Prof. Dr. Giulia Ronchi (Department of Clinical and Biological Sciences, Neuroscience Institute Cavalieri Ottolenghi, Turin)
- Prof. Dr. Axel Schambach (Institute of Experimental Hematology, MHH)
- Prof. Dr. Kerstin Schwabe (Department of Neurosurgery, MHH)
- Prof. Dr. Meike Stiesch (Department of Prosthetic Dentistry and Biomedical Materials Science, MHH)
- PD Dr. Bettina Wiegmann (Lower Saxony Center for Biomedical Engineering, Implant Research and Development, NIFE)
Experimentelle Methoden:
- Organotypische Hirngewebekulturen
- Whole-Cell-Patch-Clamp-Ableitungen an einzelnen Zellen
- Hochauflösende konfokale Mikroskopie, Analyse der synaptischen Mikroarchitektur
- Elektronenmikroskopie
- Zytokin-Profilanalysen
- Single-Nucleus-Sequenzierung
- CRISPR/Cas-basierte Geneditierung
Wir sind von der besonderen Innovationskraft kooperativer Forschung überzeugt.
Bei Interesse an einer Zusammenarbeit wenden Sie sich bitte an Prof. Dr. Maximilian Lenz.