Bitte beachten:
Vorbeugende Instandhaltungsmaßnahmen der Reinraumanlage des CTC 2026
Vom 09. Juli 2026 bis einschließlich 15. Juli 2026 können wir eine den gesetzlichen Vorgaben entsprechende Herstellung grundsätzlich nicht gewährleisten.
Davon betroffen sind alle Verarbeitungen. Weitere Informationen finden Sie hier.
Die Abgaben kryokonservierter Präparate sowie die Durchführung zellulärer Qualitätskonrollen sind davon nicht betroffen.
___________________________________________________________________________________________________________
Dienstleistungen
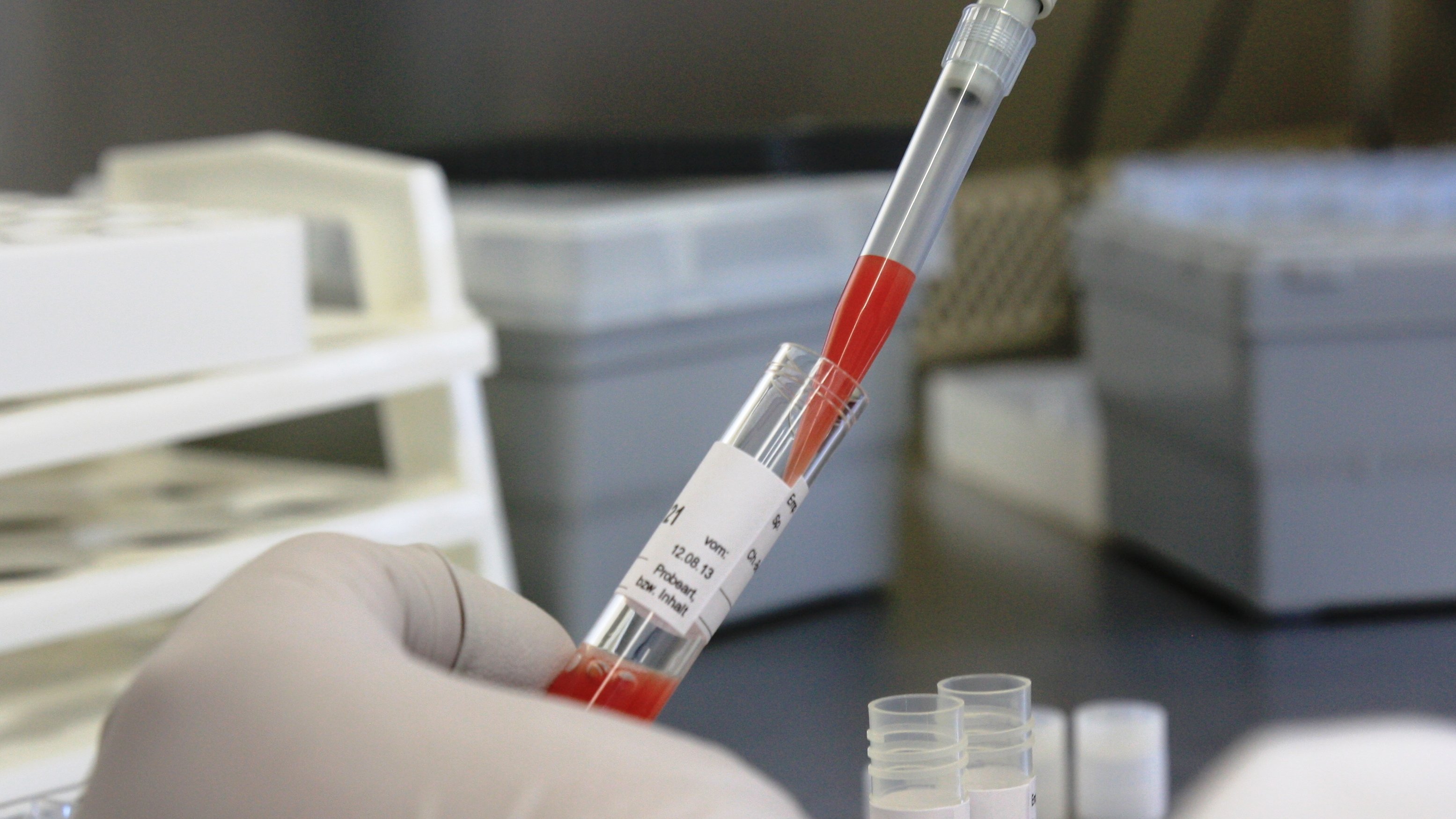
Wir stellen Arzneimittel her, die individuell auf die Patienten und deren schwere Erkrankungen, insbesondere des blutbildenden Systems, zugeschnitten sind. Präparate des CTC enthalten als aktive Bestandteile funktionale Zellen des peripheren Bluts oder des Knochenmarks.
Nachdem diese in Entnahmeeinrichtungen im In- und Ausland von den Patienten selbst, von deren Verwandten oder aber von Dritten gewonnen wurden, können wir „im Reagenzglas“ unerwünschte zelluläre oder flüssige Bestandteile entfernen, erwünschte Zellarten anreichern oder aktivieren, und, sofern erforderlich, danach das entweder bearbeitete oder weitgehend native Produkt portioniert einfrieren und tiefkalt über Jahre bis zu seiner Anwendung durch unsere klinischen Partner aufbewahren.
Zur Vermeidung einer Verunreinigung unserer Zubereitungen mit zum Beispiel Bakterien oder Viren werden die Patienten und Spender zuvor aufwendig untersucht und erfolgen relevante Bearbeitungsschritte in den CTC-eigenen Reinräumen. Ständige umfangreiche Überwachung dieser Herstellungsumgebung und des beteiligten Personals, der Ausgangspräparate und ‑materialien, der während der Prozessierung anfallenden Zwischen- und Nebenprodukte und nicht zuletzt des Arzneimittels (und schließlich der zur Überwachung angewandten Methoden selbst) sichern dessen optimale Qualität GMP-konform. Damit deren Sicherheit und Wirksamkeit kein Zufall ist.



Auftragserteilung | Formulare
Beauftragen Sie Apheresen und Präparationen sowie die Auslieferung kryokonservierter Produkte mit der jeweils aktuellen Version unserer gelenkten Formulare.
Standardpräparate/Immunselektion/-depletion
Seit 2011 liegen folgende zum Inverkehrbringen notwendigen Genehmigungen nach §21a AMG der zuständigen Bundesoberbehörde, des Paul-Ehrlich-Instituts (PEI), vor.
Erweiterte Aufarbeitungen
Zusätzlich zu unseren bereits vom Paul-Ehrlich-Institut genehmigten Arzneimittelstärken befinden sich anspruchsvolle neue Verfahren zur präparativen Immunselektion und -depletion in unterschiedlichen Stadien der Etablierung und Validierung.
Sonstige Dienstleistungen
Auf Grundlage unserer langjährigen Erfahrungen in den Bereichen Good Manufacturing Practice, Arzneimittel für neuartige Therapien, aseptische Herstellung sowie zelluläre Analytik stehen wir Ihnen schulend, beratend und gutachterlich aber auch praktisch bei Prozessetablierung und -validierung bei Ihren Projekten zur Seite – Reinraumkapazität eingeschlossen.