Projektvorstellung 2021
In sero veritas: Ein neues Werkzeug für die Forschung Hepatitis C Virus Impfstoffforschung
HCV, eine globale Bedrohung
Weltweit sind ca. 58 Millionen Menschen mit dem Hepatitis C Virus (HCV) infiziert. Wird die Infektion nicht behandelt, kann sie zu schweren Lebererkrankungen wie Leberfibrose, Zirrhose und Leberkarzinomen führen. Obwohl wirksame Behandlungen zur Verfügung stehen, bleiben viele Infizierte undiagnostiziert oder haben keinen Zugang zu einer angemessenen Behandlung. Demzufolge sterben jedes Jahr etwa 300.000 Menschen an den Folgen einer chronischen HCV-Infektion, und jedes Jahr gibt es 1,5 Millionen Neuinfektionen. Eine Impfung die vor einer Ansteckung schütze ist nicht verfügbar.
HCV-Variabilität erschwert die Entwicklung wirksamer Impfstoffe
Die Entwicklung eines Impfstoffs gegen HCV ist unter anderem deshalb so schwierig, weil das Virus extrem variabel ist. Tatsächlich können sich verschiedene Virusstämme auf Sequenzebene an mehr als 30% der Positionen unterscheiden.
Die Rolle von neutralisierenden Antikörpern für die Bewertung der Wirksamkeit von HCV-Impfstoffen
Viele Impfstoffe bieten Schutz vor Virusinfektionen, weil sie eine starke Antikörper-Reaktion hervorrufen. Aus diesem Grund ist die Analyse der Wirksamkeit von Antikörpern ein wichtiges Werkzeug, um die Qualität eines Impfstoffes einzuschätzen.
Hepatitis C reference viruses highlight potent antibody viral functional interactions
Video abstract
Objective: Neutralising antibodies are key effectors of infection-induced and vaccine-induced immunity. Quantification of antibodies’ breadth and potency is critical for understanding the mechanisms of protection and for prioritisation of vaccines. Here, we used a unique collection of human specimens and HCV strains to develop HCV reference viruses for quantification of neutralising antibodies, and to investigate viral functional diversity.
Conclusions: Representative isolates from six neutralisation clusters broadly reconstruct the functional HCV neutralisation space. They enable high resolution profiling of HCV neutralisation and they may reflect viral functional and antigenic properties important to consider in HCV vaccine design.
HCV-Referenzviren für die Bewertung neutralisierender Antikörper
Bei einem Virus so variabel wie HCV ist es besonders wichtig, die Wirkung von Antikörpern nicht nur gegen einen einzelnen HCV-Typen zu überprüfen. Sonst besteht die Gefahr sehr Virustyp-spezifische Antikörper zu priorisieren und besonders wertvolle Antikörper-„Alleskönner“, die gut gegen viele verschiedene Virustypen wirken, zu übersehen. Nur wie wählt man unter den vielen HCV-Varianten am besten einige HCV-Typen aus, um ausgewogen eine breite Wirksamkeit von Antikörpern zu messen?
Um diese Frage zu beantworten, haben wir zunächst 13 genetisch sehr unterschiedliche HCV-Varianten kloniert. Diese Viren gehören fünf der acht am weitesten verbreiteten HCV-Genotypen an und decken deswegen ein sehr weites Spektrum der genetischen Diversität des Virus ab (Abbildung 1). In einem nächsten Schritt führten wir mit diesen Viren Neutralisationstest mit polyklonalen Antikörpern von 101 HCV-positiven Patienten, die mit verschiedenen HCV-Varianten infiziert waren, durch (Abbildung 2). Diese Neutralisationsdaten wurden mit einem bioinformatischen Verfahren ausgewertet (metrische multidimensionale Skalierung).
Abbildungen
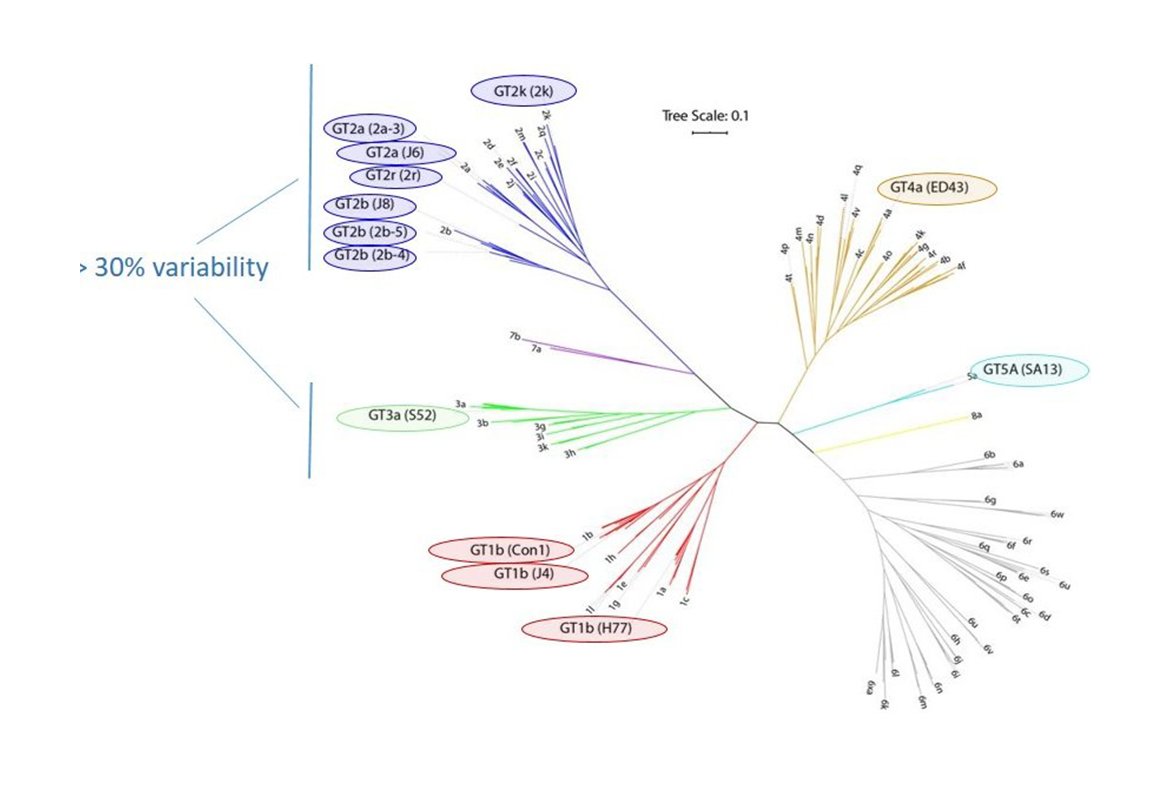
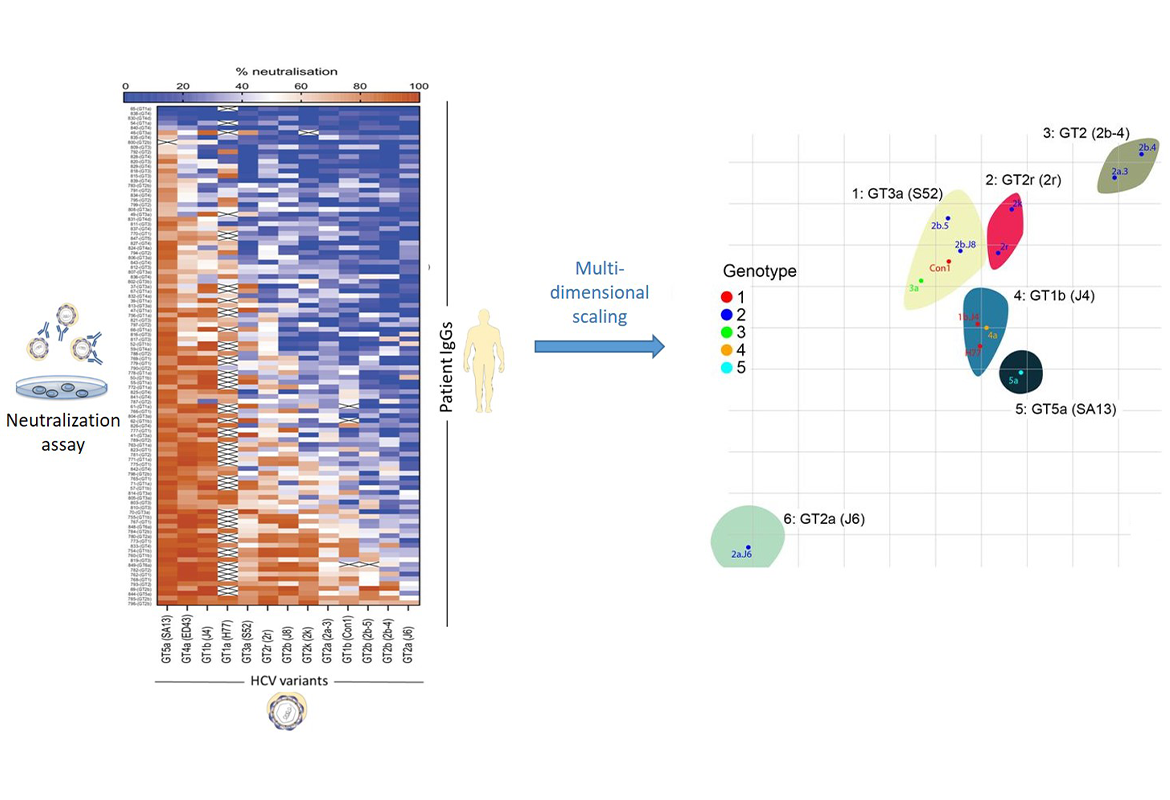
Diese Analyse ergab, dass die untersuchten Virusstämme in sechs verschiedene Gruppen eingeteilt werden können, die wir als virale Neutralisierungsbiotypen (NBT) bezeichnet haben Diese NBT lassen sich nicht anhand genetischer Sequenzvergleiche vorhersagen, sondern repräsentieren unterschiedliche funktionelle Eigenschaften der Virus-Hüllproteine bezüglich der humanen Antikörper (Bankwitz et al. Gut 2021).
Darüber hinaus haben wir dieses Verfahren eingesetzt, um Patienten aufzufinden, die besonders gute Antikörper gegen das Virus bilden („elite neutralizers“) und um die Eigenschaften ihrer Antikörper zu beschreiben (Weber et al. Immunity 2021).
Potenzial für die Entwicklung eines HCV-Impfstoffs
Diese Ergebnisse bringen das Feld der HCV-Impfstoffforschung in zweierlei Hinsicht voran: Einerseits verfügen wir jetzt über ein robustes Testsystem und einen Goldstandard für die Detektion der Antikörperreaktionen.
Andererseits hat diese Studie sechs Neutralisierungsgruppen identifiziert (NBTs), die höchstwahrscheinlich verschiedene Funktionszustände der HCV E1/E2-Proteine darstellen.
Um breit wirksame Impfstoffe zu entwickeln könnte es von Vorteil sein, diese unterschiedlichen Hüllproteintypen der sechs NBTs zu berücksichtigen anstatt einfach genetisch unterschiedliche Viren als Vakzine-Cocktail zu verwenden.
Publikationen
Hepatitis C reference viruses highlight potent antibody responses and diverse viral functional interactions with neutralising antibodies
Bankwitz D, Bahai A, Labuhn M, Doepke M, Ginkel C, Khera T, Todt D, Ströh LJ, Dold L, Klein F, Klawonn F, Krey T, Behrendt P, Cornberg M, McHardy AC, Pietschmann T. Gut. 2021 Sep;70(9):1734-1745. doi: 10.1136/gutjnl-2020-321190. Epub 2020 Dec 15. PMID: 33323394; PMCID: PMC8355883.
Analysis of antibodies from HCV elite neutralizers identifies genetic determinants of broad neutralizationWeber T, Potthoff J, Bizu S, Labuhn M, Dold L, Schoofs T, Horning M, Ercanoglu MS, Kreer C, Gieselmann L, Vanshylla K, Langhans B, Janicki H, Ströh LJ, Knops E, Nierhoff D, Spengler U, Kaiser R, Bjorkman PJ, Krey T, Bankwitz D, Pfeifer N, Pietschmann T, Flyak AI, Klein F. Immunity. 2022 Feb 8;55(2):341-35
Weitere Informationen
Herausgeber:
Präsident der MHH
Herr Prof. Dr. med. Michael P. Manns
Forschungsdekan der MHH
Herr Prof. Dr. med. Frank M. Bengel
Bearbeitung und Ansprechpartner:
Forschungsdekanat der Medizinischen Hochschule Hannover
Petra Linke
Telefon: 0511/ 532– 6023
Fax: 0511/ 532– 6024
E-Mail: linke.petra@mh-hannover.de
Gestaltung:
Digitale Medien, Medizinischen Hochschule Hannover
Telefon: 05 11/ 532– 2963
Online Umsetzung:
Forschungsdekanat, Medizinische Hochschule Hannover
Jan Tauwaldt
und
Petra Linke
Telefon: 0511/ 532- 6023
Forschungsbericht 2021
Hier finden Sie den mit Hilfe des Forschungsinformationssystems (FIS) erstellten Forschungsbericht. Wie in den vergangenen Jahren möchten wir hier die Gelegenheit nutzen, explizit ein Projekt stellvertretend vorzustellen.
Forschungsinformationssystem (FIS)Hier finden Sie weitere Informationen zum Forschungsinformationssystem (FIS).
Hochschulbibliographie- Projektvorstellung 2021
- Projektvorstellung 2020
- Projektvorstellung 2019
- Projektvorstellung 2018
- Projektvorstellung 2017
- Forschungsbericht 2016
- Forschungsbericht 2015
- Forschungsbericht 2014
- Forschungsbericht 2013
- Forschungsbericht 2012
- Forschungsbericht 2011
- Forschungsbericht 2010
- Forschungsbericht 2009
- Forschungsbericht 2008
- Forschungsbericht 2007